
聯係亚洲线精品一区二区三区八戒
電話:
021-66126658
021-66126659
盧總:
139-1700-9455
昆山電話:
0512-5759 1865
郵箱:
sy.lu@cy-water.com
地址:上海市普陀區曹楊路1700號辰金高尚領域T9幢308室
癌症免疫治療未來發展的新方向
最近,癌症免疫治療未來發展的新方向,癌症免疫療法取得多項進展,包括:靶向多種途徑的雙特異性抗體,條件激活前藥,靶向特定的免疫細胞,而這些代表了癌症免疫治療未來發展的新方向。
靶向多種途徑的雙特異性抗體
幾十年來,研究人員一直致力於研究雙特異性抗體,該類藥物有望成為癌症治療新類別。由於最近的進展,雙特異性抗體已接近臨床。
Genmab公司副總裁、晚期腫瘤轉化負責人Maria N. Jure-Kunkel博士說:“廣泛的臨床前和現在的早期臨床數據表明,可能需要針對多種互補的免疫途徑來激發強大的抗腫瘤免疫力並改善患者的預後。”
Genmab的DuoBody®平台通過快速且廣泛適用的工藝產生雙特異性抗體,該工藝可輕鬆在發現規模和商業製造規模上進行。DuoBody®分子的獨特之處在於將雙特異性的優勢與傳統抗體的優勢相結合,這使得DuoBody®分子可以作為其他抗體治療劑進行給藥。
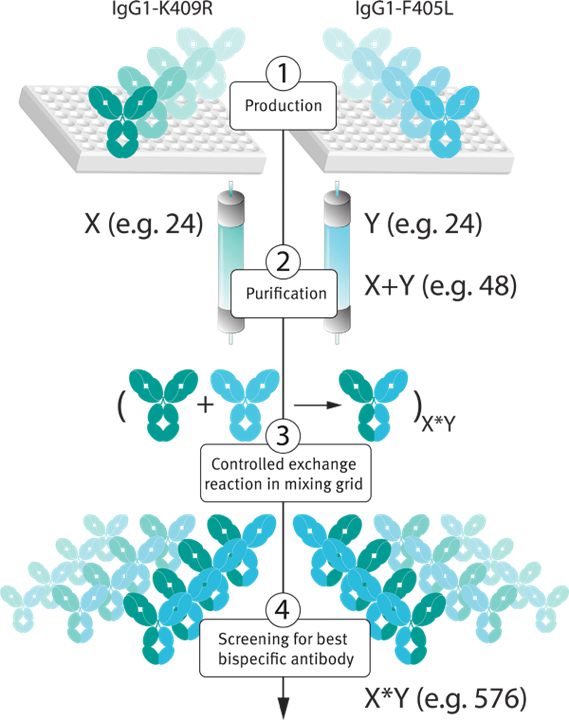
圖1:DuoBody®平台生成雙特異性抗體庫
Genmab與合作夥伴BioNTech一起,正在開發兩種新的研究療法,即GEN1046/BNT311和GEN1042/BNT312,具有共刺激受體激動劑活性。這些研究性雙特異性抗體旨在通過共同靶向關鍵免疫途徑來解決抗腫瘤免疫缺陷或次優的問題。這個想法是部署一個可以作用於調節抗腫瘤免疫反應的兩種不同途徑的單一分子。
共刺激受體的條件激活意味著當雙特異性分子的兩個靶點都參與時,這些受體的激活被嚴格引發,因為信號隻有在受體交聯時才會發生,正如在臨床前研究中觀察到的那樣,由於雙重靶向導致的條件性可能將活性定位在重要的腫瘤微環境和相關淋巴結中,從而解決臨床中觀察到的激動性抗體的一些局限性。
GEN1046/BNT311通過同時和互補的PD-L1阻斷以及條件性4-1BB刺激引發抗腫瘤免疫反應,後者屬於腫瘤壞死受體家族。4-1BB是一種可誘導的T細胞共刺激受體,在活化的CD4+和CD8+T細胞以及活化的自然殺傷細胞上表達。同時阻斷PD-L1/PD1和4-1BB激活可改善T細胞功能並促進腫瘤細胞的殺傷。
GEN1046目前正處於實體瘤的I/II期臨床研究和作為單一藥物或與其他標準治療療法聯合用於複發/難治性轉移性非小細胞肺癌II期臨床研究中。
GEN1042靶向於CD40以及4-1BB。CD40的靶向增強了樹突狀細胞和抗原依賴性T細胞的活化。根據正在進行的首次人體研究的初步數據,GEN1042顯示出良好的安全性,並在經過大量預處理、異質的患者群體中鼓勵早期臨床活動。GEN1042與標準護理療法的聯合治療正在實體瘤中進行I/II期臨床研究。
模塊化CAR-T細胞成開啟實體瘤“金鑰匙”
嵌合抗原受體(CAR)T細胞療法已在化療難治性B細胞癌的持久緩解方麵取得突破性進展。然而,由於多種挑戰,包括TME的免疫抑製影響,CAR-T細胞療法對實體瘤的使用受到限製。
Autolus Therapeutics正在解決這些挑戰,該公司正在開發針對實體瘤癌症的CAR-T細胞療法,特別是神經母細胞瘤。
該公司的治療候選藥物之一AUTO6NG是一種靶向GD2的CAR-T細胞係統,GD2是一種在大多數神經母細胞瘤中大量表達但在正常組織中基本不存在的二唾液酸神經節苷脂。AUTO6NG由兩個共同轉導的工程模塊化載體組成。
第一個載體旨在提高CAR-T細胞的持久性,而第二個載體支持CAR-T細胞在TME中的功能。兩種載體的共同點是靶向GD2的CAR-T細胞模塊。據該公司稱,這種方法在沒有伴隨神經毒性的患者中顯示出高抗腫瘤活性。
條件激活前藥
前藥是一種具有吸引力的癌症免疫治療方法。全身給藥的前藥在到達腫瘤微環境(TME)之前可能保持無活性,在TME被激活並啟動強大的抗腫瘤反應。說起來容易做起來難度卻很大。一個常見的問題是腫瘤異質性阻止了前藥被充分激活。
為了克服這個問題,Werewolf Therapeutics正在利用蛋白質工程技術Predator來製造名為Indukines的有條件激活分子。該公司聲稱其Indukines可以增強腫瘤特異性殺傷,同時最大限度地減少不良的脫靶效應。
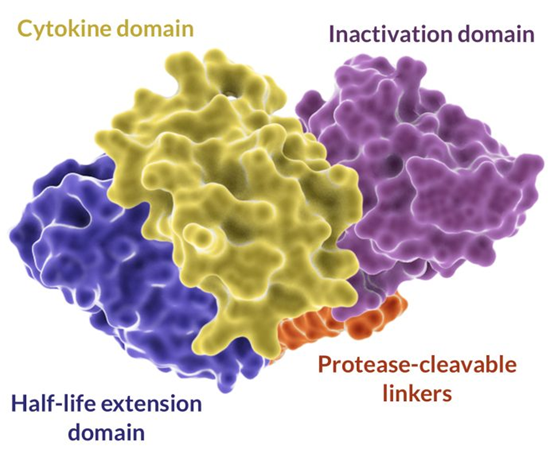
圖2:Werewolf Therapeutics開發的腫瘤激活免疫治療前藥
Indukine分子旨在釋放腫瘤的促炎機製,同時防止對非靶組織產生不良副作用。典型的Indukine由野生型細胞因子(例如,IL-2或IL-12)、阻斷外周活性的失活結構域、在腫瘤微環境中激活的腫瘤蛋白酶敏感接頭和半衰期延長結構域組成。
該公司的一種IL-2Indukine分子WTX-124前藥已在臨床前研究中顯示出前景。WTX-124通過激活腫瘤浸潤性CD8+和CD4+T細胞表現出有效的抗腫瘤活性,並且相對於重組人IL-2具有更好的治療窗。
Werewolf Therapeutics另一款IL-12Indukine分子WTX-330前藥,由於其對免疫細胞的多效性作用,WTX-330可能成為治療耐藥類型癌症的遊戲規則改變者。
該公司的科學家最近證明,WTX-330可以重新編程腫瘤浸潤性CD8+T細胞,以推動多個同基因腫瘤模型中的腫瘤消退,並且該藥可以擴大治療窗口(與重組IL-12相比)。WTX-330也被證明在免疫原性較低的腫瘤模型中具有活性。
WTX-124和WTX-330預計將在今年晚些時候進入I期臨床試驗。
靶向特定的免疫細胞
阿地白介素(Aldesleukin)是實驗室製造的一種IL-2,用於治療黑色素瘤或腎細胞癌成人患者。事實上,第一代高劑量阿地白介素的全身治療可以通過增加T細胞和B細胞的活性和生長來幫助免疫係統殺死癌細胞。然而,該藥物有幾個局限性:反應率低(僅為15%);毒性顯著(包括毛細血管滲漏綜合征);治療指數狹窄;半衰期短;以及調節性T細胞(Tregs)的優先擴增。
羅氏製藥研究和早期開發(pRED)小組的研究人員正在解決其中的一些限製。例如,他們通過將高親和力抗PD-1抗體與修飾的IL-2變體(IL-2v)融合,開發了一種嵌合抗體細胞因子蛋白。與野生型IL-2不同,IL-2v不與IL-2受體亞基α(IL-2Ra)結合。IL-2Ra也稱為CD25。CD25作為Treg細胞表麵的特異性標誌物之一,是靶向Treg細胞的潛在靶點。利用CD25抗體特異性殺傷Treg細胞,進而解除免疫抑製,被視為抗腫瘤治療的重要途徑。
PD1-IL-2v通過順式機製發揮作用,與表達IL-2R同一細胞上PD-1結合。值得注意的是,PD-1在TCR激活後也由腫瘤特異性T細胞表達。通過利用IL-2v向PD-1+T細胞的順式遞送,可以將IL-2R激動從CD25表達細胞轉向PD-1表達細胞。
PD1-IL-2v是第一個開發的靶向PD-1的IL-2Rbg偏向激動劑,現在正在I期試驗(NCT04303858)中對其進行評估。
上一個: 【重磅】如何執行醫療器械注冊自檢
下一個: 製藥純化水設備選購的注意事項


